「珍藏版」综述 | 细胞铁死亡,肿瘤放疗,以及联合治疗
发布时间:2024-09-16
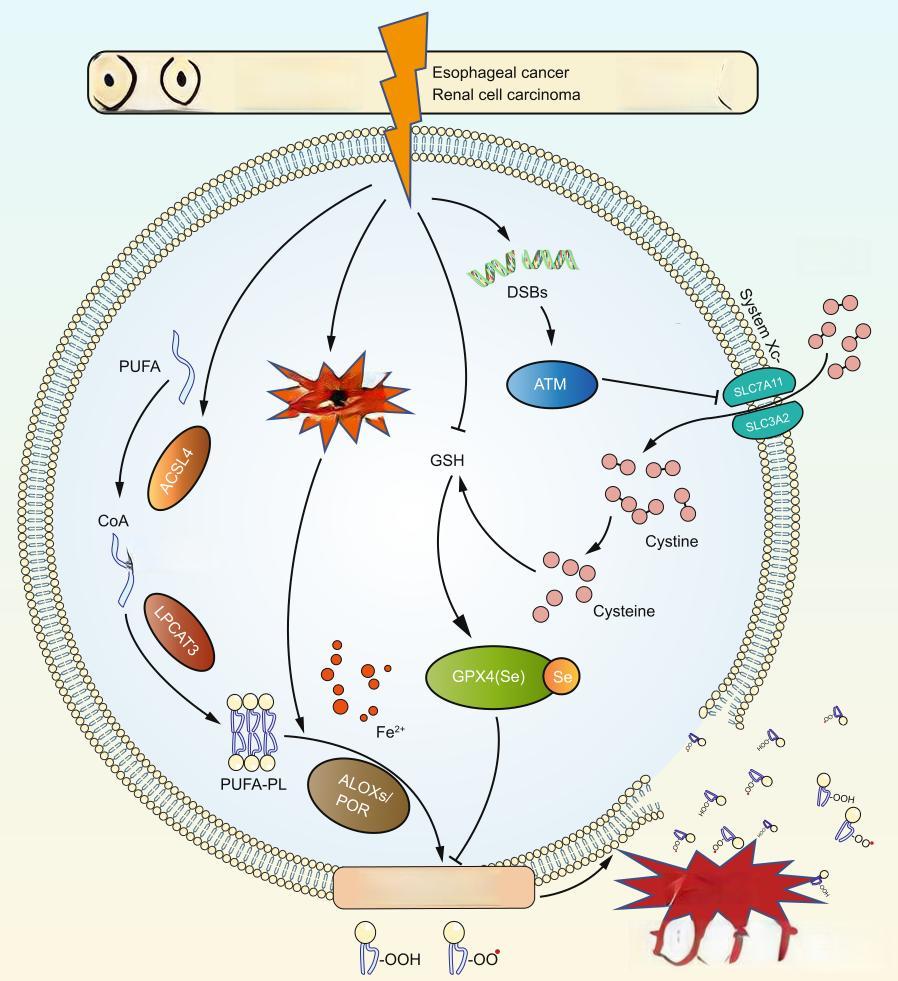
细胞铁死亡是一种新兴的细胞程序性死亡方式 ,近年来在肿瘤放疗领域引起了广泛关注。这种死亡方式依赖于铁离子的积累,其形态学改变和发生机制均不同于凋亡、坏死、自噬等其他形式的细胞死亡。
铁死亡的本质是谷胱甘肽的耗竭和脂质氧化物的积累 。在正常情况下,细胞通过谷胱甘肽过氧化物酶4(GPX4)将具有细胞毒性的过氧化氢磷脂还原为无毒的脂醇,减少脂质过氧化作用。然而,当GPX4活性下降时,细胞膜上脂质过氧化物会致命性积累,导致细胞膜破裂和崩解,最终引发铁死亡。这一过程还涉及到细胞内铁离子的异常积累,过量的Fe2+通过芬顿反应氧化脂质产生大量活性氧(ROS),进一步加剧脂质过氧化。
在肿瘤放疗中,铁死亡扮演着重要角色 。研究发现,放疗能诱导铁死亡标志基因环加氧酶2(PTGS2)的表达,放疗后的细胞出现了典型的铁死亡形态学特征。使用铁死亡抑制剂可以部分恢复放疗后细胞的存活,这表明铁死亡是放疗诱导细胞死亡的重要机制之一。
利用铁死亡来增强肿瘤放疗效果成为了一个新的研究方向 。例如,通过抑制细胞内的铁代谢平衡,可以增加肿瘤细胞对放疗的敏感性。一项研究显示,在放射性肠炎小鼠模型中,通过铁螯合或缺铁饮食来缓解肠上皮细胞中的铁超载,能够减轻小肠黏膜损伤,提高小鼠在接受致死剂量的全腹放疗后的存活率。
然而,铁死亡在放疗中的作用并非单一。一方面,它可能增强放疗效果;另一方面,它也可能导致正常组织的放射损伤。例如,在放射性肺损伤模型中,铁死亡的特征性表现包括线粒体收缩、ROS升高、GPX4减低等。这提示我们,在设计基于铁死亡的放疗增强策略时,需要权衡其对肿瘤细胞和正常组织的不同影响。
目前,关于铁死亡与放疗的研究还存在一些局限性。大多数研究集中在动物和细胞水平,缺乏临床安全性和有效性的评估。此外, 铁死亡的具体调控机制仍有待进一步阐明 。未来的研究需要更多地关注铁死亡在人体放射性损伤中的防护作用,以及如何在不影响肿瘤细胞放射敏感性的情况下,特异性地限制铁死亡抑制剂在正常细胞中的作用。
总的来说,细胞铁死亡为肿瘤放疗提供了一个新的视角和潜在的治疗策略。通过深入理解铁死亡的机制及其与放疗的相互作用,我们有望开发出更有效的放疗方案,提高肿瘤治疗的效果,同时减少对正常组织的损伤。