科学家发现FcuR形式免疫球蛋白M的分子机制,助力理解生物学功能
发布时间:2024-09-18
免疫球蛋白M(IgM)是人体内最早产生的抗体 ,被誉为体液免疫的“先锋部队”。然而,长期以来,IgM与其特异性受体FcμR之间的相互作用机制一直是个谜。近日,北京大学肖俊宇教授团队在Nature杂志上发表的最新研究成果,终于揭开了这一神秘面纱。
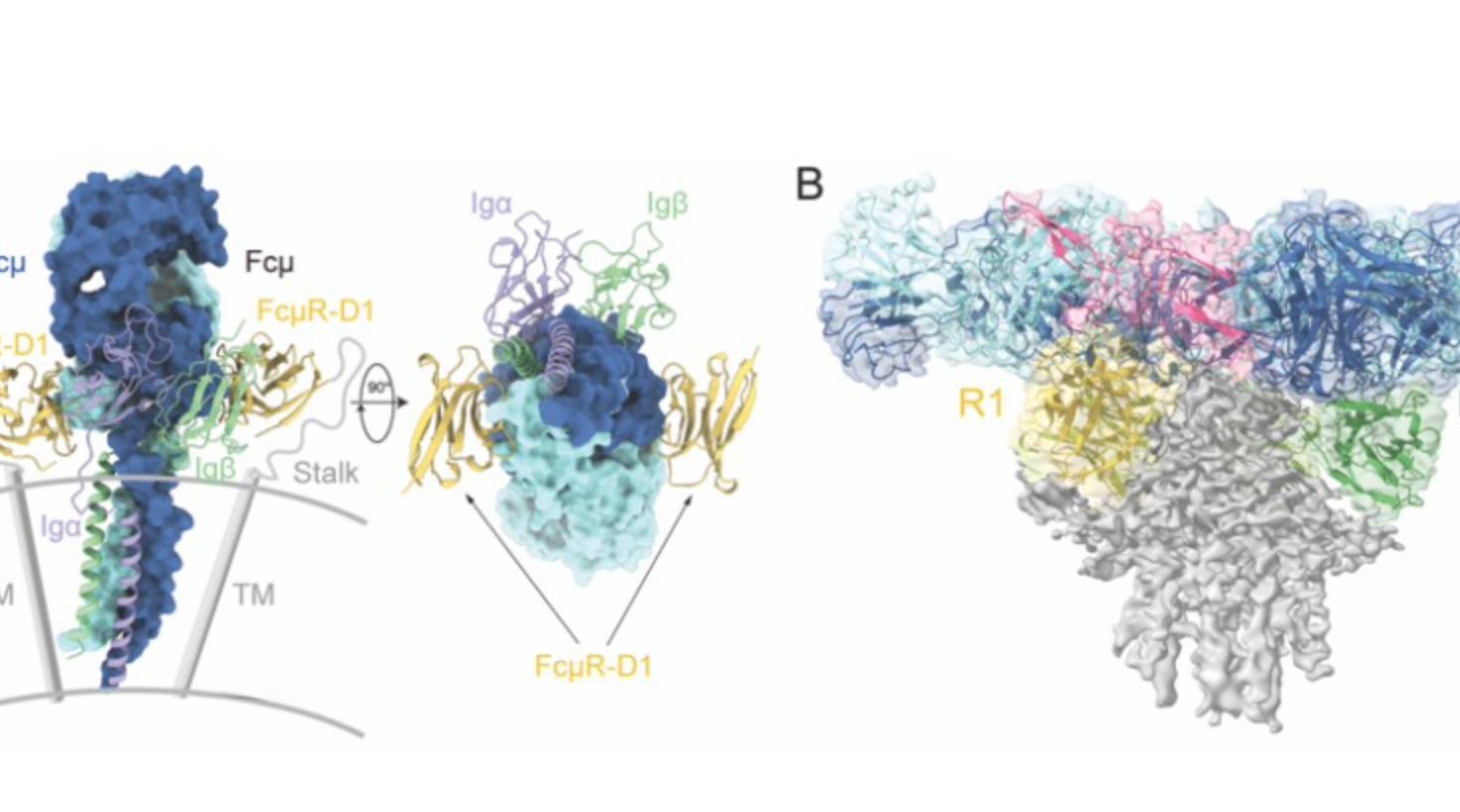
肖俊宇团队通过结构生物学、生物化学和细胞生物学等手段,揭示了FcμR如何特异性地识别和结合不同形式的IgM。研究发现,[FcμR的胞外域包含一 研究发现,FcμR的胞外域包含一个Ig样结构域(D1结构域)和一段高度糖基化的Stalk区。 在与IgM相互作用时,2个FcμR-D1结构域会分别结合在1个IgM-Cμ4二聚体的两侧,形成2:1的复合物。这种结合方式与之前的研究结果一致,证实了每个IgM重链都含有一个FcμR结合点。
更有趣的是, 当研究团队利用冷冻电镜技术解析IgM五聚体与FcμR的复合体结构时,他们发现了两种不同的结合模式:1:1和4:1。 在1:1模式中,单个FcμR-D1与分泌型IgM(sIgM)中的分泌成分(SC)占据相似的位置,与IgM的J链相互作用。而在4:1模式中,4个FcμR分子同时结合在IgM五聚体的同一侧,暗示IgM五聚体可能通过诱导FcμR形成四聚体来启动下游信号传导。Stalk区可能进一步介导4个FcμR分子之间的相互作用,促进其结合于IgM的同一侧。
这一发现不仅揭示了FcμR识别不同形式IgM的复杂机制,也为理解IgM的生物学功能奠定了基础。 IgM作为最早产生的抗体,在感染早期的免疫应答中起着关键作用。 它具有强大的杀菌、激活补体、免疫调理和凝集作用,同时也参与某些自身免疫病及超敏反应的病理过程。FcμR作为IgM的特异性受体,主要存在于B细胞表面,在T细胞等其他免疫细胞表面也有表达。它不仅参与B细胞的发育和免疫系统的稳态调控,还在慢性淋巴细胞白血病(CLL)等疾病中扮演重要角色。
肖俊宇团队的研究成果为深入理解IgM的生物学功能提供了新的视角,也为相关疾病的治疗提供了新的思路。例如, 基于FcμR与IgM相互作用的机制,科学家们可以设计靶向FcμR的免疫疗法 ,用于治疗CLL等B细胞恶性肿瘤。此外,这项研究还为开发新型疫苗和抗体药物提供了理论基础。
展望未来,IgM和FcμR的研究仍有广阔的空间。科学家们需要进一步探索FcμR在免疫调节中的具体作用机制,以及它如何影响IgM的生物学功能。同时,利用这些新发现开发更有效的免疫治疗方法也将是未来研究的重点。随着研究的深入,我们有望揭开更多关于人体免疫系统的奥秘,为人类健康事业做出更大贡献。