细胞活力检测方法大盘点,CTG法放大招?
发布时间:2024-09-18
细胞活力检测是生命科学研究中不可或缺的重要手段。从早期的MTT法到如今的CTG发光法,细胞活力检测技术经历了显著的演变。这一发展历程不仅反映了科研需求的不断升级,也体现了技术创新对生命科学研究的深远影响。
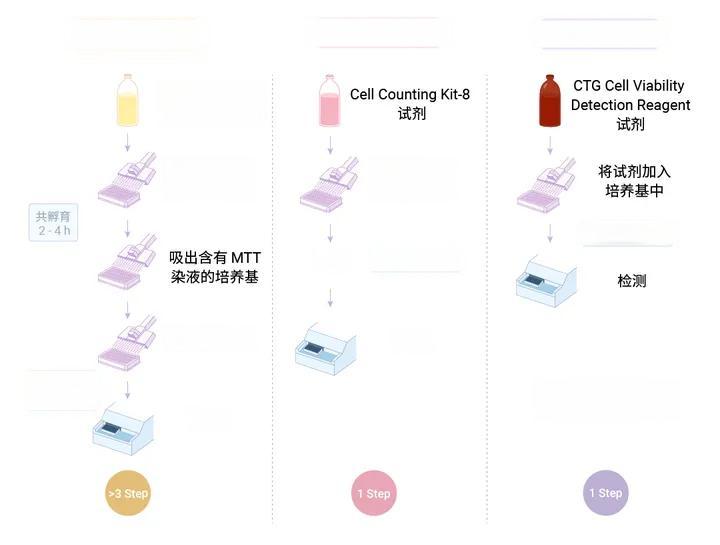
MTT法作为细胞活力检测的“元老”,自20世纪80年代问世以来,便因其操作简便、成本低廉而被广泛采用。其原理是利用活细胞线粒体中的琥珀酸脱氢酶将MTT还原为不溶于水的蓝紫色结晶Formazan,通过测定490 nm处的吸光值来间接反映细胞活力。然而,MTT法也存在明显缺陷:操作耗时,需要DMSO溶解Formazan,且DMSO对人体具有毒性。
随着技术进步,CCK8法应运而生。CCK8是一种基于WST-8的比色检测方法,相比MTT法在操作步骤和检测时间上都有所优化。但CCK8法仍然存在一个令人困扰的问题:“细胞增殖越多越快,则颜色越深;细胞毒性越大,则颜色越浅”,这种颜色深浅的标准难以精确量化。
在这一背景下,CTG发光法的出现堪称细胞活力检测领域的“放大招”。CTG法基于高灵敏度生物发光检测技术,通过定量三磷酸腺苷(ATP)来测定培养物中活细胞数目及细胞活力。这种方法可以用三个字概括:“快、准、狠”。与MTT法相比,CTG法的处理速度提高了近20倍,节省时间近4小时。其特有的均质检测法——“加样-混样-检测”,使得操作变得异常简单。
CTG法的优势不仅体现在操作简便上,更在于其高灵敏度和广泛适用性。ATP作为细胞新陈代谢的重要指标,与活细胞数目呈良好线性关系。CTG法通过测定ATP含量来进行细胞计数或活力测定,且不受化合物自发荧光的影响。这使得CTG法成为细胞增殖测定、细胞活力测定和细胞毒性高通量筛选的理想选择。
在实际应用中,CTG法已经展现出强大的潜力。例如,在研究SIPL1对三阴性乳腺癌(TNBC)细胞增殖的影响时,研究人员使用CTG法进行细胞增殖检测。结果显示,转染靶向SIPL1 shRNAs的BT-549和MDA-MB-231细胞系的细胞增殖显著降低。这一发现为理解SIPL1在TNBC中的作用机制提供了重要线索。
另一个典型案例是,研究人员在探究外源RRM2对肝癌细胞铁死亡的影响时,通过CTG法检测细胞活力。结果表明,过表达RRM2时,细胞活力明显增强;反之,敲除RRM2时,细胞活力明显降低。这一发现为理解RRM2在肝癌发展中的作用提供了新的视角。
CTG法在高通量筛选中的应用同样引人注目。在一项针对疟原虫肝脏和无性血期寄生虫的活性化合物筛选研究中,研究人员使用CTG法评估了4,253种化合物对HepG2细胞的细胞毒性。最终,他们筛选出994种经过验证的无毒性化合物,用于后续的抗疟原虫活性评估。
CTG法之所以能在短时间内获得科研人员的青睐,与其独特的优势密不可分。首先,CTG法的操作极其简便,只需“加样-混合-读数”即可完成检测,大大缩短了检测时间。其次,CTG法具有极高的灵敏度,线性范围宽,甚至可以检测到低至10个数量的细胞。此外,CTG法的发光信号持久,半衰期长达3-5小时,非常适合高通量筛选的需求。
尽管CTG法展现出诸多优势,但我们也要认识到,没有一种方法可以完美适用于所有场景。在选择细胞活力检测方法时,科研人员仍需根据具体研究需求和条件,权衡各种方法的优缺点,做出最适合的选择。
细胞活力检测方法的演变历程,从MTT法到CTG法,不仅反映了技术的进步,更体现了科研需求的不断升级。随着生命科学研究的深入,我们有理由相信,未来还会有更多创新的细胞活力检测方法涌现,为生命科学的发展提供更强大的技术支持。