CDE文章 | 浅析化学药品贮藏条件的制定
发布时间:2024-09-03
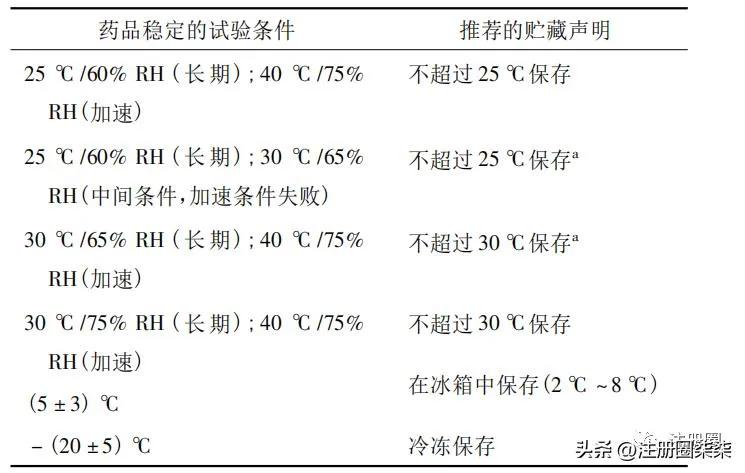
药品贮藏条件对药品质量、安全性和有效性有着重要影响。不当的贮藏条件可能导致药品变质,增加用药风险。然而,我国在化学药品贮藏条件的制定和管理方面仍存在一些问题,需要进一步完善。
目前,我国关于药品贮藏条件的法规和技术指南涵盖了药品研发、注册及上市后流通等全生命周期。2015年发布的《化学药品原料药和制剂稳定性研究指导原则》要求基于全面的稳定性信息评估制定贮藏条件,避免使用“环境条件”或“室温”等不确切表述。《药品说明书和标签管理规定》则规定了具体温度的标注要求。然而,与欧美等发达国家相比,我国在这一领域的法规和技术指南仍显不足。
美国和欧盟的相关法规和技术指南更为详细。美国联邦法规21CFR Sec. 201对药品说明书和标签的内容和格式有明确规定,要求描述特殊处理和贮藏条件。欧盟委员会发布的《产品特征概要(SmPC)撰写指南》则要求列出未开启包装和已开启、稀释或复溶的无菌药品的贮藏条件。相比之下,我国的法规和技术指南在具体指导药品贮藏条件制定和规范撰写方面的作用有限。
在药典方面,《中华人民共和国药典》凡例中收载的贮藏条件较为有限,缺少“冷冻”条件,且“冷处”温度范围(2℃~10℃)与国际通行的冷藏长期稳定性条件(5±3℃)不匹配。此外,我国多数药品说明书还缺少儿童防开启或防触及的提醒,可能导致用药安全性风险。
具体到药品贮藏条件的制定和规范撰写,我国化学药品存在以下问题:贮藏条件表述不规范,如“4℃以下保存”等;同一品种不同厂家贮藏条件不一致;同一品种国内外贮藏条件不一致;稳定性研究数据不充分;缺少儿童防开启或防触及的提醒等。
针对这些问题,化学药品贮藏条件的制定应遵循以下基本原则:综合药品稳定性试验结果和流通过程中可能遇到的情况;确保每一项贮藏要求均有稳定性数据支持;仿制药的贮藏条件应参照参比制剂制定,不能简单降低贮藏条件以掩盖质量不一致;境外已上市药品在国内上市销售时,应根据稳定性数据确定贮藏条件,不能简单翻译境外获批贮藏条件。
在书写规范方面,应使用规范术语描述,对光照敏感的药品应包括遮光/避光要求,建议注明具体温度并增加上下限,必要时通过包装避免药品受潮。贮藏条件应按照光照、包装状态、温度和特殊贮藏要求的顺序列出。
为确保药品质量,保障用药安全,业界和监管机构应共同努力,完善药品贮藏条件的制定和管理。药品上市许可持有人作为第一责任人,应根据准确规范的研究结果科学制定药品贮藏条件,并进行全生命周期管理。监管机构则应进一步完善和细化相关法规和技术指南体系建设,国家药典委员会也应完善《中华人民共和国药典》凡例中贮藏相关规定,加强与主流国家药典的协调。
只有通过多方协作,才能有效防止潜在的贮藏相关用药风险,保障人民群众用药安全。