巧用“信号兵”拓荒“处女地”!中国科学家首次阐明黏附类受体自发激活分子机制
发布时间:2024-09-15
G蛋白偶联受体(GPCR)是人体内最大的药物靶标蛋白家族,超过40%的上市药物通过作用于这些受体发挥疗效。然而,在这个庞大的家族中,仍有约100种GPCR的配体和信号转导通路不明,这些被称为“孤儿受体”的成员成为药物研发的“处女地”。
黏附类GPCR就是这样一个充满挑战的领域。这个包含33种受体的家族参与调控免疫反应、器官发育和细胞通讯等重要生理过程,与精神分裂症、多动症和癌症等多种疾病密切相关。然而,由于其复杂的分子结构和未知的功能机制,黏附类GPCR的研究进展一直缓慢。
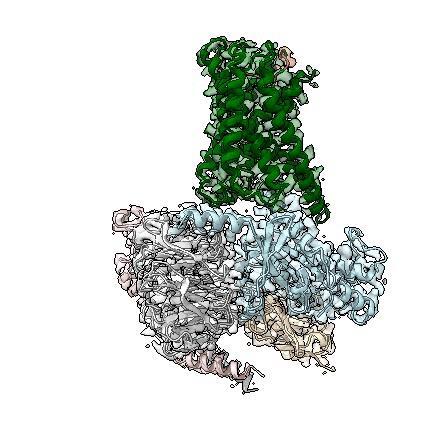
近日,中国科学院上海药物研究所吴蓓丽研究组、赵强研究组联合上海科技大学水雯箐研究组在这一领域取得了突破性进展。他们成功解析了两种黏附类GPCR(ADGRD1和ADGRF1)分别与G蛋白结合的复合物三维结构,并首次阐明了这类孤儿受体自发激活的分子机制。
研究发现,黏附类GPCR的自激活机制与已知的GPCR截然不同。在其他类型的GPCR中,受体通常需要外界配体的刺激才能激活。而黏附类GPCR则可以通过自身结构的变化实现自激活。具体来说,位于受体胞外结构域和跨膜结构域之间的一段多肽(称为“stalk”)可以作为内源性激动剂,通过与跨膜结构域作用,导致跨膜螺旋发生构象变化,从而激活受体。
更令人惊讶的是,研究团队发现stalk的自剪切并非激活所必需。这一发现颠覆了以往对黏附类GPCR功能的认识,为理解这类受体的信号转导机制提供了全新的视角。
此外,研究还首次发现细胞膜的脂质成分溶血磷脂胆碱(LPC)可以与GPCR结合并对受体功能发挥调控作用。这一发现极大地拓展了我们对GPCR功能调控机制的认识。
这些突破性成果为黏附类GPCR的药物研发提供了重要依据。研究团队表示,这些结构和功能信息为药物设计提供了精准的模板,将有助于靶向这两种黏附类受体的癌症治疗药物开发。
复旦大学教授徐彦辉评价道:“这些研究充分体现黏附类GPCR信号转导和调控机制的独特性、复杂性和多样性,促进对这类受体分子机制的理解,为研究大量结构、功能未知的孤儿受体提供了新思路,也为挖掘其药物研发潜力提供了新线索。”
这一研究不仅揭示了黏附类GPCR的神秘面纱,也为孤儿GPCR的研究开辟了新天地。随着对这些“处女地”的深入探索,我们有望发现更多潜在的药物靶点,为治疗多种疾病带来新的希望。中国科学家在这一领域的领先贡献,再次彰显了中国在基础研究和创新药物研发方面的实力。