高三化学总复习,热方程式的判断与书写,这个分你能拿到吗?
发布时间:2024-09-03
在高三化学总复习中,热化学方程式常常让许多学生感到困惑。然而,如果我们将其视为化学反应的“能量密码”,就能更好地理解和掌握这个知识点。
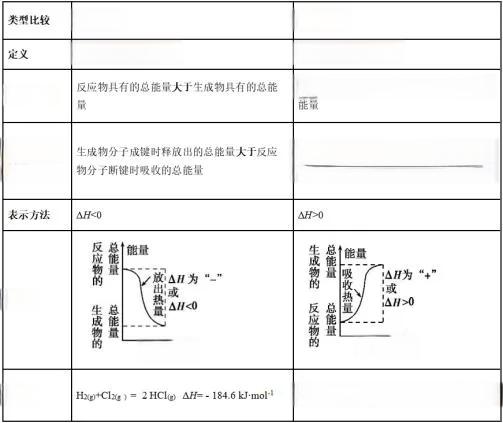
热化学方程式不仅是普通化学方程式的升级版,它还揭示了化学反应中的能量变化。正如一把钥匙能打开一扇门,一个正确的热化学方程式能揭示反应的全部秘密 - 物质变化和能量变化。例如,H2(g) + Cl2(g) = 2HCl(g) ΔH(298K) = -184.6 kJ/mol 这个方程式告诉我们,在298K时,1 mol氢气和1 mol氯气完全反应生成2 mol氯化氢气体,会放出184.6 kJ的热量。
要正确书写这个“能量密码”,我们需要记住几个要点:
- 标明物质状态:用(g)、(l)、(s)等符号标明反应物和生成物的状态。
- 注明温度和压强:通常默认为298K和101kPa,但特殊情况下需要明确标注。
- 正确使用ΔH:放热反应ΔH为负值,吸热反应ΔH为正值。
- 化学计量数:可以是整数或分数,表示物质的量,而不是分子数。
然而,许多学生在书写热化学方程式时会犯一些常见错误。例如,忘记标注物质状态,或者错误地使用ΔH的正负号。记住,一个小小的错误可能会导致整个“密码”失效,无法正确解读反应的秘密。
热化学方程式的真正威力在于它的应用 - 尤其是盖斯定律。这个定律告诉我们,不管化学反应是一步完成还是分几步完成,其反应热是相同的。这就像是解密的“万能钥匙”,让我们可以通过间接途径计算难以直接测量的反应热。
让我们通过一个例子来说明如何应用这个“能量密码”:
已知:
- H2(g) + 1/2O2(g) = H2O(l) ΔH(298K) = -285.8 kJ/mol
- H2O(l) = H2(g) + 1/2O2(g) ΔH(298K) = +285.8 kJ/mol
现在,我们要计算H2O(g) = H2(g) + 1/2O2(g)的ΔH。虽然我们没有直接的实验数据,但我们可以利用盖斯定律来间接计算:
H2O(l) = H2(g) + 1/2O2(g) ΔH(298K) = +285.8 kJ/mol
H2O(l) = H2O(g) ΔH(298K) = +44 kJ/mol
将这两个反应相加,我们得到:
H2O(g) = H2(g) + 1/2O2(g) ΔH(298K) = +329.8 kJ/mol
这就是热化学方程式的魅力所在 - 它不仅揭示了化学反应的物质变化,还揭示了能量变化,让我们能够更深入地理解化学反应的本质。掌握这个“能量密码”,你就能在化学考试中轻松应对热化学方程式相关的题目,拿到高分不再是梦想。