探寻丙酮酸脱氢酶复合酶系研究进展
发布时间:2024-09-18
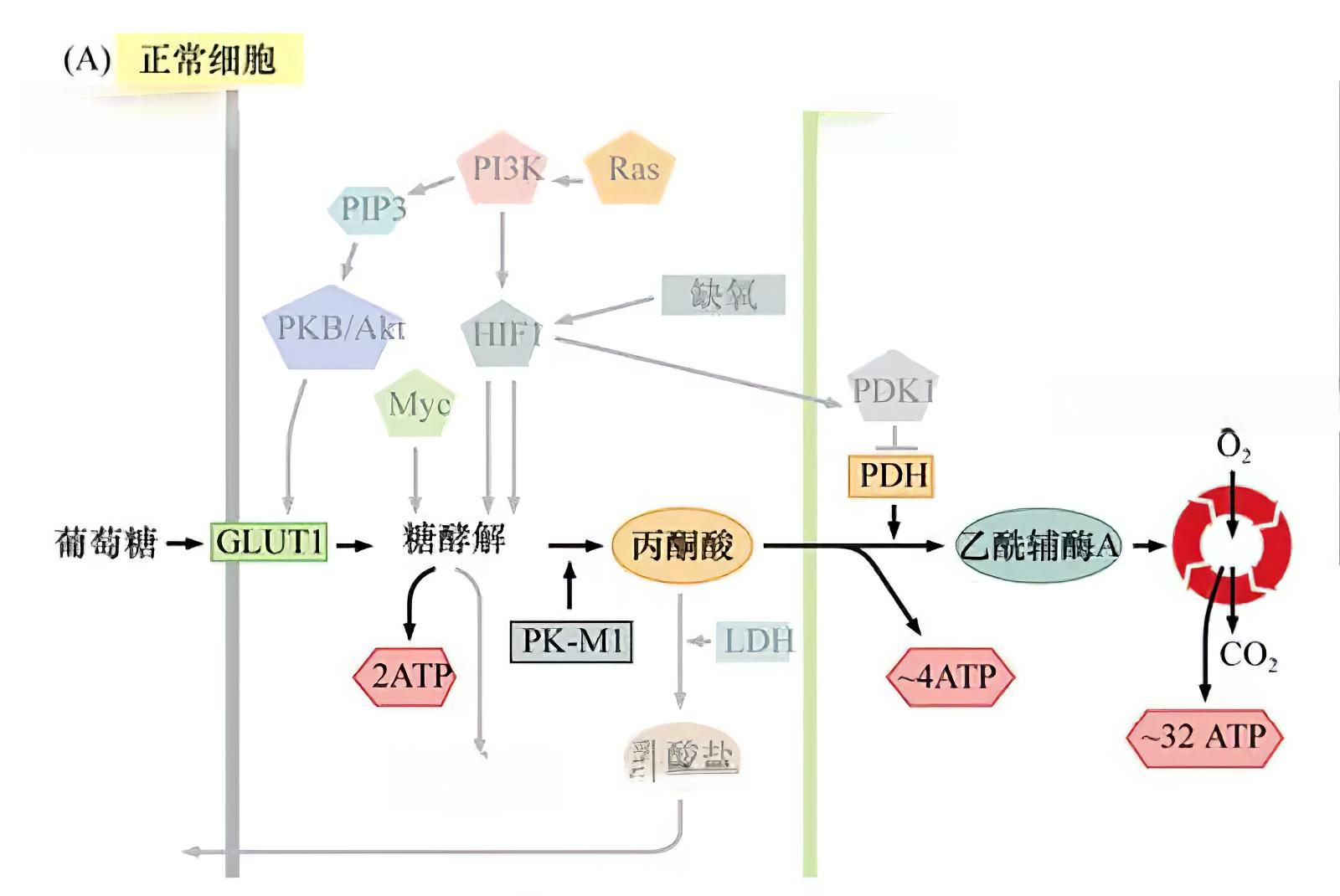
丙酮酸脱氢酶复合酶系(PDH complex)作为连接糖酵解和三羧酸循环的关键酶 ,在肿瘤细胞代谢中扮演着至关重要的角色。近年来,随着对肿瘤代谢特征的深入研究,PDH复合酶系在癌症发生发展中的作用逐渐引起科学家们的关注。
肿瘤细胞通常表现出活跃的糖酵解代谢特征,即使在氧气充足的条件下也是如此。这种被称为“瓦堡效应”的现象,早在20世纪20年代就被德国科学家奥托·瓦堡观察到。 瓦堡效应不仅为肿瘤细胞提供了快速增殖所需的能量,还为其生物合成提供了必要的原料。 然而,这种代谢方式的维持需要抑制PDH复合酶系的活性,从而减少丙酮酸进入三羧酸循环的量。
丙酮酸脱氢酶激酶(PDK)在这一过程中起到了关键作用。PDK能够磷酸化并抑制PDH复合酶系的活性,从而促进糖酵解。研究表明,肿瘤细胞中PDK的表达通常增加,导致PDH复合酶系活性降低,进而维持了肿瘤细胞的糖酵解代谢模式。
最近,中国科学院分子细胞科学卓越创新中心杨巍维研究组的一项突破性研究揭示了PDH复合酶系在肿瘤免疫逃逸中的新功能。研究发现, PDH复合酶系E1组分α亚基(PDHE1α)不仅在线粒体中发挥催化作用,还存在丰富的胞质定位。 胞质PDHE1α通过促进磷脂酶PPM1B对IKKβ的去磷酸化,削弱了NF-κB信号通路的激活,增强了炎症因子及细胞毒性T淋巴细胞(CTLs)诱导的肿瘤细胞死亡。
然而,当MAPK等致癌信号被激活时,胞质PDHE1α的S327位点会被ERK2磷酸化并转位到线粒体。这一过程导致胞质PDHE1α水平下降,恢复了NF-κB信号通路的活化;同时,线粒体PDHE1α的增多提升了α-酮戊二酸的含量,并促进炎症因子刺激下肿瘤细胞的ROS解毒。NF-κB的活化和ROS的清除共同促进了肿瘤细胞在炎症因子刺激下的存活,增强了肿瘤细胞对CTLs的耐受性,最终促进了肿瘤的免疫逃逸和抗PD-1治疗的耐药性。
这一发现不仅揭示了PDHE1α亚细胞转位调控肿瘤免疫逃逸的新机制,还为开发新型抗癌策略提供了新的思路。研究者们指出, 抑制PDHE1α的磷酸化可能成为阻断肿瘤免疫逃逸、提高肿瘤免疫治疗疗效的新途径。
此外,研究还发现肺癌患者肿瘤组织中PDHE1α S327磷酸化水平与胞质PDHE1α水平、ERK2活性和NF-κB激活相关;胞质PDHE1α水平或PDHE1α S327磷酸化水平与肺癌患者的恶性程度和预后相关。这些发现为PDHE1α作为潜在的肿瘤诊断和预后标志物提供了依据。
总的来说,丙酮酸脱氢酶复合酶系在肿瘤代谢和免疫逃逸中的关键作用,使其成为了一个极具潜力的抗癌靶点。未来针对PDH复合酶系的药物开发,可能会为癌症治疗带来新的突破。然而,要将这些研究成果转化为临床应用,还需要更多的基础研究和临床试验来验证其安全性和有效性。