靶向Aurora B激酶增强BIM和PUMA介导的细胞凋亡克服EGFR抑制剂耐药
发布时间:2024-09-15
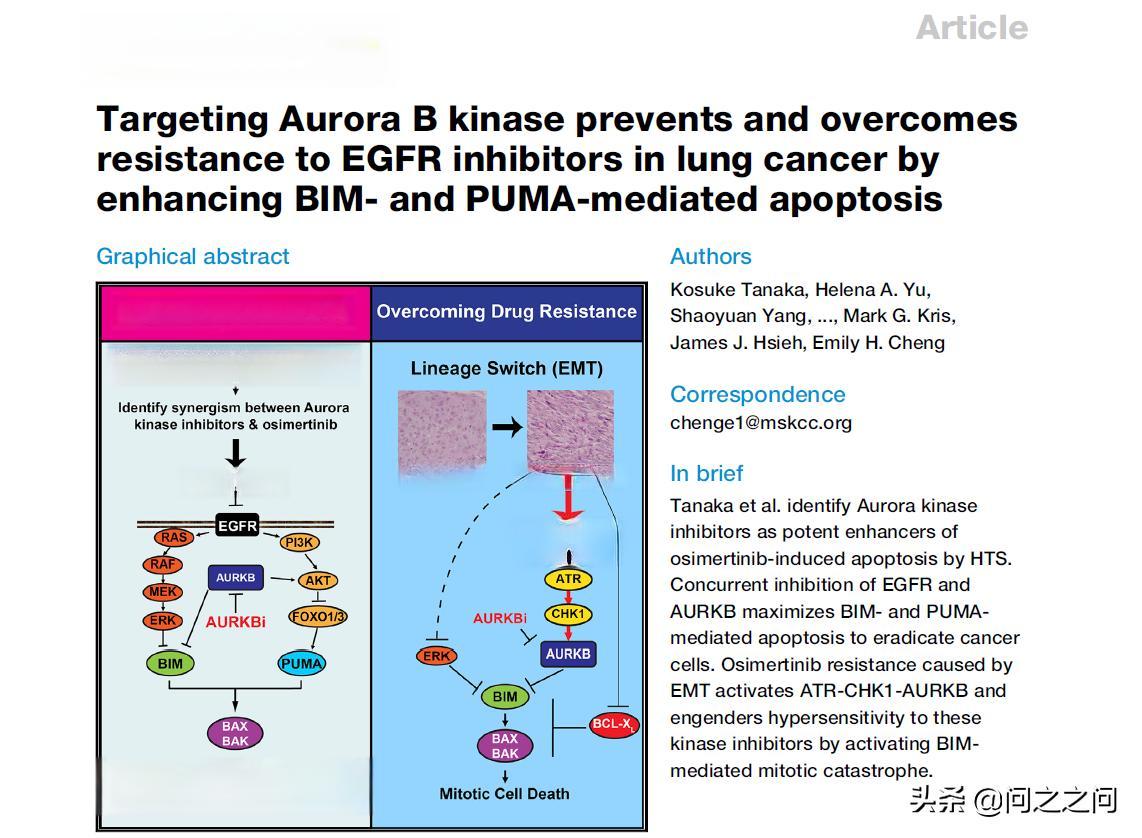
Aurora B激酶在细胞周期中扮演着关键角色,它参与调控细胞有丝分裂过程中的中心体成熟、纺锤体组装和染色体分离等重要步骤。然而,这把“双刃剑”在癌症治疗中既可能成为敌人,也可能成为盟友。
在多种实体瘤中,Aurora激酶(包括Aurora B)常常过度表达,导致异常的有丝分裂和基因不稳定性,从而促进肿瘤的发生和增殖。这使得Aurora激酶成为了一个极具潜力的抗肿瘤靶点。目前,一些Aurora激酶抑制剂已经进入临床试验阶段,并显示出较强的抗肿瘤活性。
然而,针对表皮生长因子受体(EGFR)的酪氨酸激酶抑制剂(TKI)在治疗非小细胞肺癌(NSCLC)时,常常面临耐药性的挑战。约50%的患者在治疗过程中会出现EGFR的T790M突变,导致药物结合位点改变,从而产生耐药性。此外,约20%的患者会出现MET原癌基因扩增,激活下游信号通路,使肿瘤细胞在TKI存在的情况下仍能存活。
面对这些耐药机制,研究人员开始探索新的治疗策略。其中一个创新思路是靶向Aurora B激酶,通过增强BIM和PUMA介导的细胞凋亡来克服EGFR抑制剂的耐药性。
BIM和PUMA是两个重要的促凋亡蛋白,它们在细胞凋亡中发挥着关键作用。有趣的是,BIM的缺失多态性已被证明会导致EGFR突变患者对TKI的敏感性下降。这提示我们,增强BIM的功能可能有助于提高治疗效果。
研究表明,Aurora B激酶的抑制可以增强BIM和PUMA介导的细胞凋亡。具体来说,Aurora B激酶的抑制可以促进BIM和PUMA的表达,从而增加细胞对凋亡的敏感性。这种机制不仅能够直接杀死癌细胞,还可能通过增强细胞凋亡来克服EGFR抑制剂的耐药性。
此外,Aurora B激酶抑制剂与EGFR抑制剂的联合使用可能产生协同效应。一方面,Aurora B激酶抑制剂可以克服T790M突变导致的耐药性;另一方面,它还可以通过增强BIM和PUMA的功能来提高细胞对EGFR抑制剂的敏感性。
尽管这一治疗策略显示出巨大的潜力,但仍面临一些挑战。例如,Aurora B激酶抑制剂可能会影响正常细胞的有丝分裂,导致不良反应。因此,开发更特异性的抑制剂,或者寻找合适的生物标志物来筛选可能受益的患者群体,将是未来研究的重点。
总的来说,靶向Aurora B激酶,增强BIM和PUMA介导的细胞凋亡,为克服EGFR抑制剂耐药性提供了一个新的思路。这一策略不仅可能提高现有治疗的疗效,还可能为开发新一代抗肿瘤药物开辟新的方向。