铅酸蓄电池的化学反应
发布时间:2024-09-02
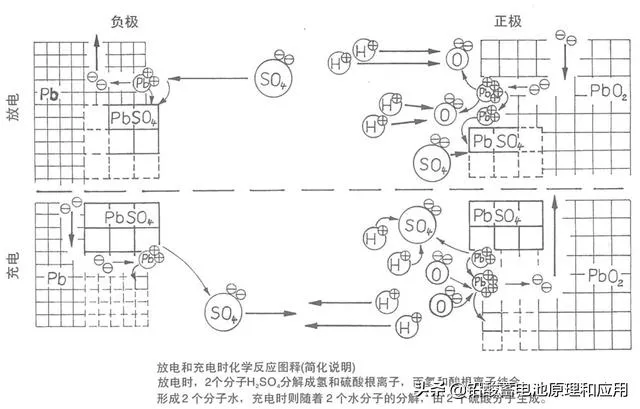
铅酸蓄电池是一种历史悠久且应用广泛的二次电池,其工作原理基于铅、二氧化铅和硫酸之间的化学反应。这种电池由正极板(二氧化铅)、负极板(铅)和电解液(硫酸溶液)组成,通过充电和放电过程实现电能和化学能的相互转换。
在放电过程中,铅酸蓄电池的正极和负极分别发生氧化还原反应。负极上,铅与硫酸反应生成硫酸铅,并释放出两个电子:
Pb + SO4^2- → PbSO4 + 2e-
正极上,二氧化铅与硫酸和水反应生成硫酸铅,同时吸收两个电子:
PbO2 + 4H+ + SO4^2- + 2e- → PbSO4 + 2H2O
这两个反应共同构成了电池的总反应:
Pb + PbO2 + 2H2SO4 → 2PbSO4 + 2H2O
随着放电的进行,电解液中的硫酸浓度逐渐降低,而硫酸铅在电极上积累,导致电池内阻增加,电动势下降。
充电过程则是放电过程的逆反应。在外加直流电源的作用下,正极板上的硫酸铅被还原为二氧化铅,负极板上的硫酸铅被还原为铅:
PbSO4 + 2e- → Pb + SO4^2-
PbSO4 + 2H2O → PbO2 + 4H+ + SO4^2- + 2e-
这两个反应共同构成了充电过程的总反应:
2PbSO4 + 2H2O → Pb + PbO2 + 2H2SO4
充电过程中,电解液中的硫酸浓度逐渐升高,电池恢复到初始状态。
铅酸蓄电池具有以下优点:首先,安全性好,即使遭受摔打也能继续使用。其次,价格低廉,约为锂离子电池的1/3。最后,可回收性强,废旧电池中的铅可以回收再利用,减少了环境污染。
然而,铅酸蓄电池也存在一些缺点:重量大,电池容量有限,寿命较短。一般来说,铅酸电池在深充深放电400次以内,寿命在三年左右。
尽管存在这些缺点,铅酸蓄电池仍然在许多领域得到广泛应用。在汽车领域,它主要用于起动、照明和点火系统。在工业领域,铅酸电池广泛应用于不间断电源(UPS)、应急照明和备用电源系统。此外,它还被用于太阳能和风能等可再生能源的储能系统中。
总的来说,铅酸蓄电池凭借其成熟的技术、低廉的价格和良好的安全性,在电池市场中占据重要地位。尽管新兴的锂离子电池在能量密度和寿命方面具有优势,但铅酸电池在性价比方面仍然具有竞争力。随着技术的不断进步,铅酸电池有望在更广泛的领域发挥重要作用。