高中化学教学设计 反应条件对化学平衡的影响
发布时间:2024-09-02
化学平衡是高中化学教学中的一个重要概念,它描述了在一定条件下,化学反应达到的一种动态平衡状态。理解反应条件对化学平衡的影响,不仅有助于学生掌握这一核心概念,还能为他们未来在化学领域的深入学习和研究奠定基础。
浓度、温度和压强是影响化学平衡的三个关键因素。以浓度为例,当增加反应物浓度时,平衡会向生成物方向移动。这一现象可以通过勒夏特列原理来解释:系统会自发地向减弱外界干扰的方向移动。具体来说,增加反应物浓度相当于增加了反应物分子的碰撞机会,从而促使更多反应物转化为生成物,直到新的平衡建立。
温度对化学平衡的影响更为复杂。对于放热反应,升高温度会使平衡向逆反应方向移动;对于吸热反应,则相反。这种现象的原理在于,温度的升高相当于向系统中加入了能量,系统会通过向吸热方向移动来“消耗”这部分额外的能量,从而达到新的平衡。
压强对化学平衡的影响主要体现在有气体参与的反应中。根据勒夏特列原理,增加压强会使平衡向体积减小的方向移动。例如,在反应N2 + 3H2 ⇌ 2NH3中,增加压强会使平衡向生成氨气的方向移动,因为生成物的气体分子数少于反应物。
值得注意的是,催化剂虽然能加快反应速率,但并不影响化学平衡的位置。这是因为催化剂同等程度地影响正逆反应速率,不会改变反应物和生成物的相对浓度。
理解这些原理对日常生活和工业生产具有重要意义。以高炉炼铁为例,工程师们曾错误地认为增加一氧化碳与铁矿石的接触时间可以提高铁的产量。然而,根据化学平衡理论,当反应达到平衡时,增加接触时间并不能改变产物的浓度。正确的做法应该是通过改变温度、压强等条件来移动平衡,从而提高铁的产量。
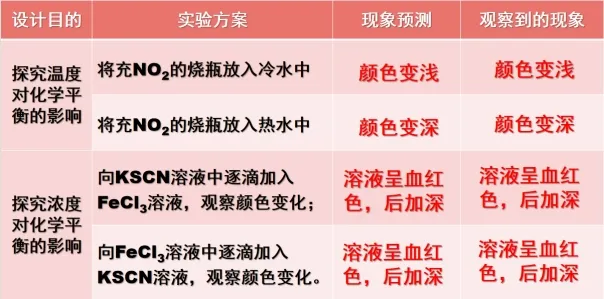
在教学中,教师可以通过设计一系列实验来帮助学生直观地理解这些原理。例如,可以通过改变FeCl3和KSCN溶液的浓度来观察溶液颜色的变化,从而理解浓度对化学平衡的影响。同时,教师还应该引导学生思考这些原理在现实生活中的应用,如如何优化工业生产过程,如何解释自然界中的化学现象等。
总之,化学平衡的教学不应局限于理论知识的传授,而应该通过实验探究、案例分析等多种方式,让学生深刻理解反应条件对化学平衡的影响,并学会运用这些原理解决实际问题。只有这样,才能真正激发学生的学习兴趣,培养他们的科学思维能力。