《AM》:膜融合介导肿瘤细胞表面工程化聚糖增强 NK 细胞治疗
发布时间:2024-09-18
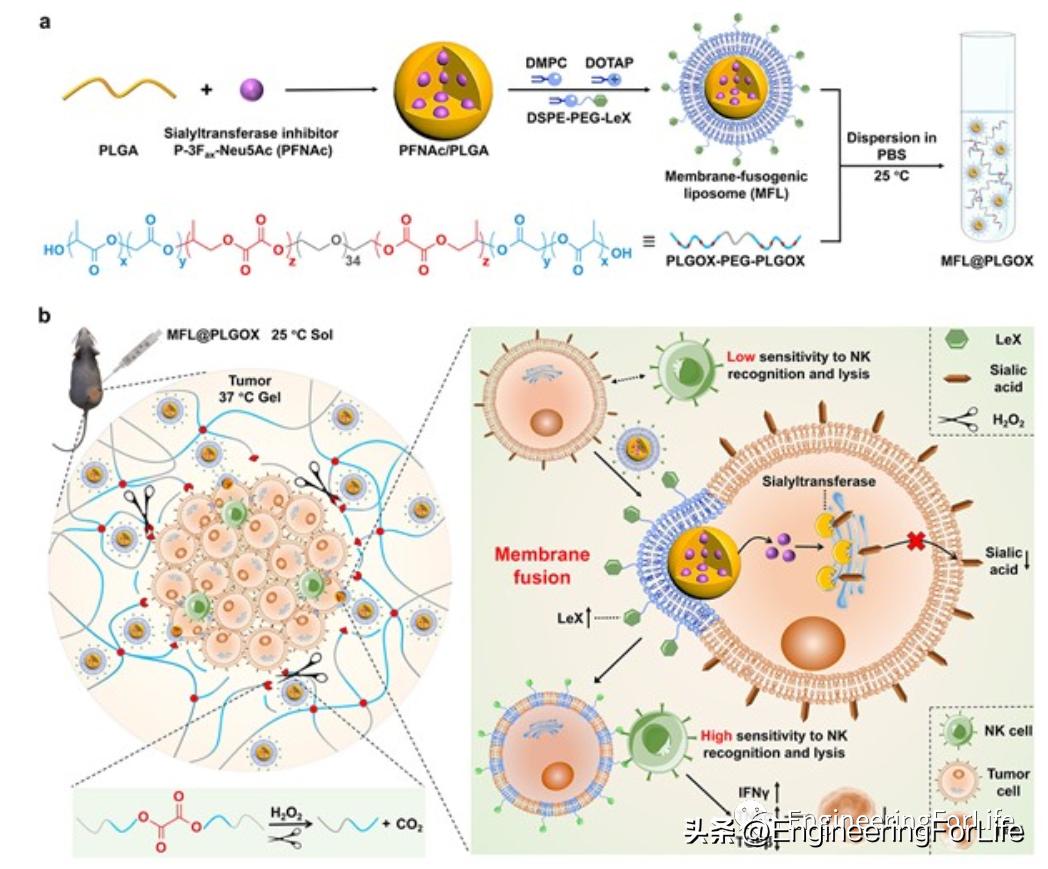
自然杀伤(NK)细胞疗法在肿瘤治疗领域展现出巨大潜力,但肿瘤细胞表面过度表达的免疫抑制聚糖严重限制了其治疗效果。为逆转这一糖介导的免疫抑制,中国科学院长春应用化学研究所陈学思团队与中山大学李明强、陶玉团队合作,开发出一种创新的 膜融合介导肿瘤细胞表面聚糖工程技术 ,为增强NK细胞治疗效果开辟了新途径。
这项研究设计了一种核-壳结构的膜融合脂质体(MFL), 通过与肿瘤细胞膜融合,同时实现肿瘤细胞表面NK活化多糖的物理修饰和免疫抑制多糖的生物抑制。 MFL的核心装载有唾液酸转移酶抑制剂(PFNAc),外壳则修饰有NK激活聚糖Lewis X三糖(LeX)。当MFL与肿瘤细胞膜融合后,PFNAc被递送到细胞质中,有效抑制细胞内唾液酸转移酶,降低表面唾液酸表达;同时,LeX被直接锚定在肿瘤细胞表面,显著增加NK细胞激活信号。
研究结果显示, MFLs使α2,3-唾液酸表达减少85.6%,α2,6-唾液酸水平减少70.0% ,同时肿瘤细胞表面的LeX表达增加4.3倍。这种表面聚糖信号的多重工程策略成功将富含唾液酸的肿瘤表面重新编程为LeX修饰的表面,充分重新激活了肿瘤浸润性NK细胞的识别和裂解能力,显著增强了抗肿瘤免疫反应。
为了实现MFLs的可控释放,研究团队将其负载到肿瘤微环境触发的可降解温敏水凝胶中,形成MFL@PLGOX复合物。这种复合物可以在室温下局部注射到肿瘤中,然后在37℃的肿瘤生理条件下快速胶凝。由于肿瘤环境中过量的H2O2,PLGOX-PEG-PLGOX骨架中的草酸盐键断裂,凝胶逐渐降解,原位释放MFLs,实现了聚糖重塑的持续优化。
在B16F10荷瘤小鼠模型中, MFL@PLGOX显著增强了NK依赖性抗肿瘤反应 ,提高了肿瘤抑制效果。当与过继NK疗法联合使用时,治疗效果进一步显著改善。这项研究不仅提出了一种新的肿瘤表面聚糖信号多重工程策略,还为细胞表面信号的多模式定制和细胞间相互作用的个性化调节提供了一种有效方法。
膜融合介导肿瘤细胞表面聚糖工程技术的成功开发,为克服传统NK细胞疗法的局限性提供了新的思路。通过直接改造肿瘤细胞表面的聚糖信号,这种方法有望提高NK细胞疗法的特异性和有效性,为癌症患者带来新的治疗希望。未来,随着这项技术的进一步优化和临床验证,我们有理由期待它将在肿瘤免疫治疗领域发挥重要作用,为癌症治疗开辟新的篇章。