谷歌DeepMind祭出蛋白质设计新AI,有望攻克癌症!蛋白亲和力暴增300倍
发布时间:2024-09-15
Google DeepMind 团队推出了一种用于设计 与目标分子结合更紧密 的新型蛋白质的 AI 系统 AlphaProteo。
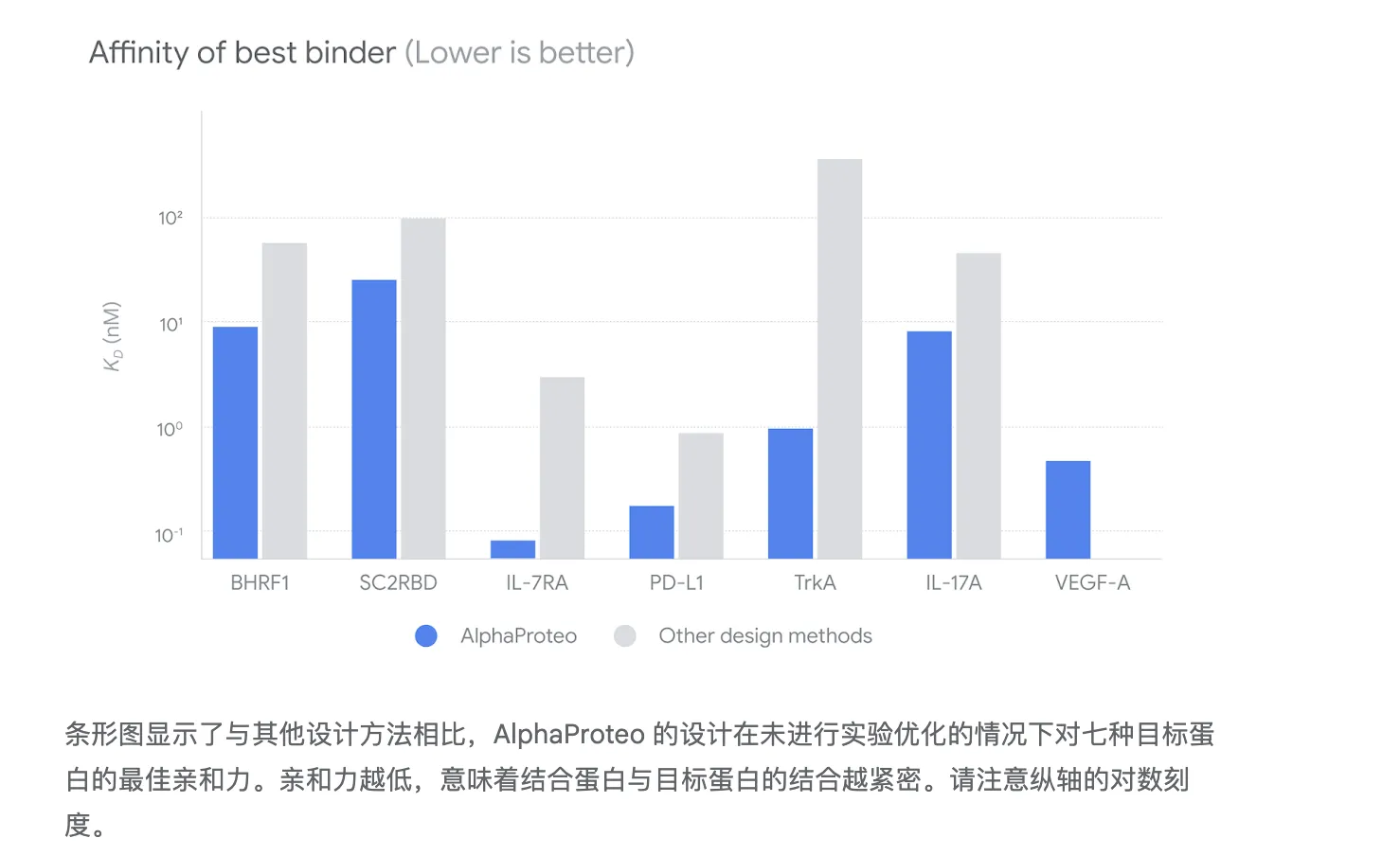
在测试的 7 种靶蛋白上,AlphaProteo 比现有最佳方法的蛋白结合亲和力高出 3 到 300倍。
AlphaProteo的意义在于,可以预防病毒感染,设计抗癌,等各种治愈疾病的药物。
通过蛋白结合剂紧密附着在「病毒」、「癌细胞」上,阻止它们之间的信号传递,扰乱其功能,使其最终走向死亡。
AlphaProteo在简化药物发现、个性化癌症治疗和加速科学研究方面有很大潜力,但它在生成某些蛋白质(如TNFɑ)结合物方面仍面临挑战和限制。
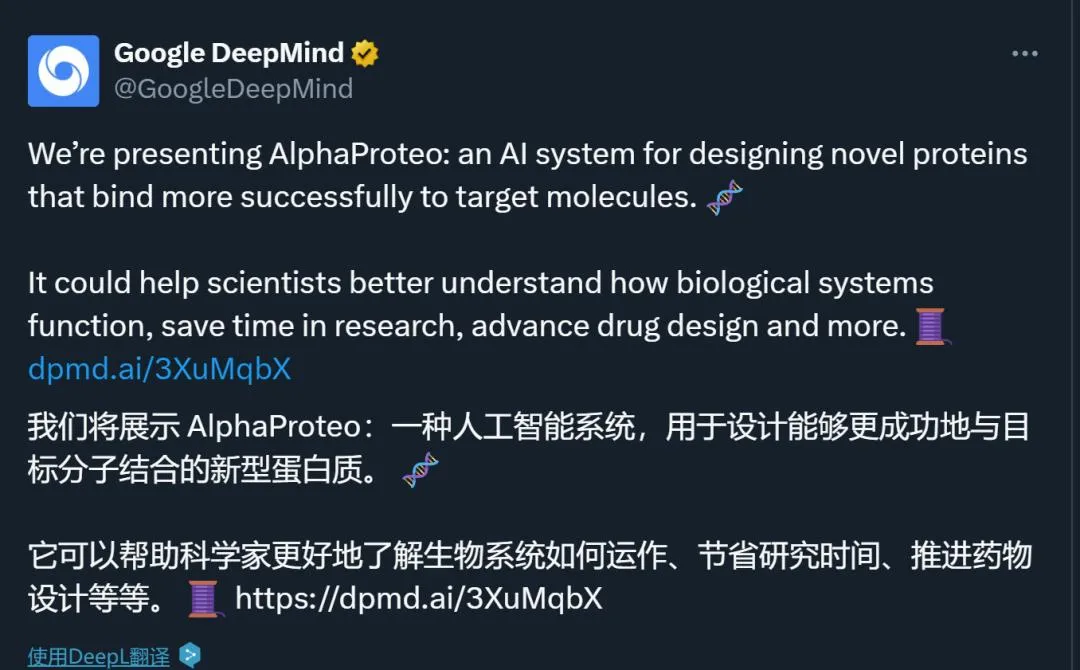
AlphaProteo简介
AlphaProteo概述
AlphaProteo是一种创新的蛋白质设计方法,采用人工智能技术来推动生物研究和新疗法的开发。
与传统的蛋白质结构预测工具不同,AlphaProteo采用了全新的方法,专门生成能够结合特定分子的全新蛋白质。
这类 蛋白质结合剂 可以加速许多领域研究的进展,包括药物开发、细胞和组织成像、疾病理解和诊断,甚至是提升作物抗虫性。

AlphaProteo的能力与局限性
AlphaProteo通过其先进的AI驱动方法,在生成针对多种目标蛋白质的高效结合物方面表现优异,包括与癌症和糖尿病并发症相关的蛋白质VEGF-A。
这标志着AI系统首次开发出针对这一关键目标的蛋白质结合物。
AlphaProteo的卓越能力不仅为研究人员提供了探索蛋白质功能的新工具,还可能引领重大的科学和医学突破。
尽管如此,AlphaProteo在创造TNFɑ结合物方面面临一定挑战,表明该系统并非完美无缺。开发团队正在致力于改进AlphaProteo,以克服这些障碍,提高其对更具挑战性目标的有效性。
蛋白质设计与疗法的未来
AlphaProteo的推出是在长达数十年的蛋白质疗法和工程发展的背景下进行的。
自1980年代初以来,重组自然蛋白质的出现及抗体类药物的发展,已成为重要的蛋白质疗法类别。
AlphaProteo的发布标志着 克服限制蛋白质生物制剂临床应用的生理障碍(例如,无法穿越细胞膜)和采用新型细胞质递送策略解决难治性疾病 的重要时刻。
随着对理解蛋白质结构和功能的重要性日益增加,AlphaProteo在药物开发中的作用被视为未来该领域进展的关键贡献,为各个领域定制蛋白质开辟了新的可能性。
AlphaProteo背后的技术创新
变革性的蛋白质设计
AlphaProteo的成功归功于AlphaFold系列的进步。
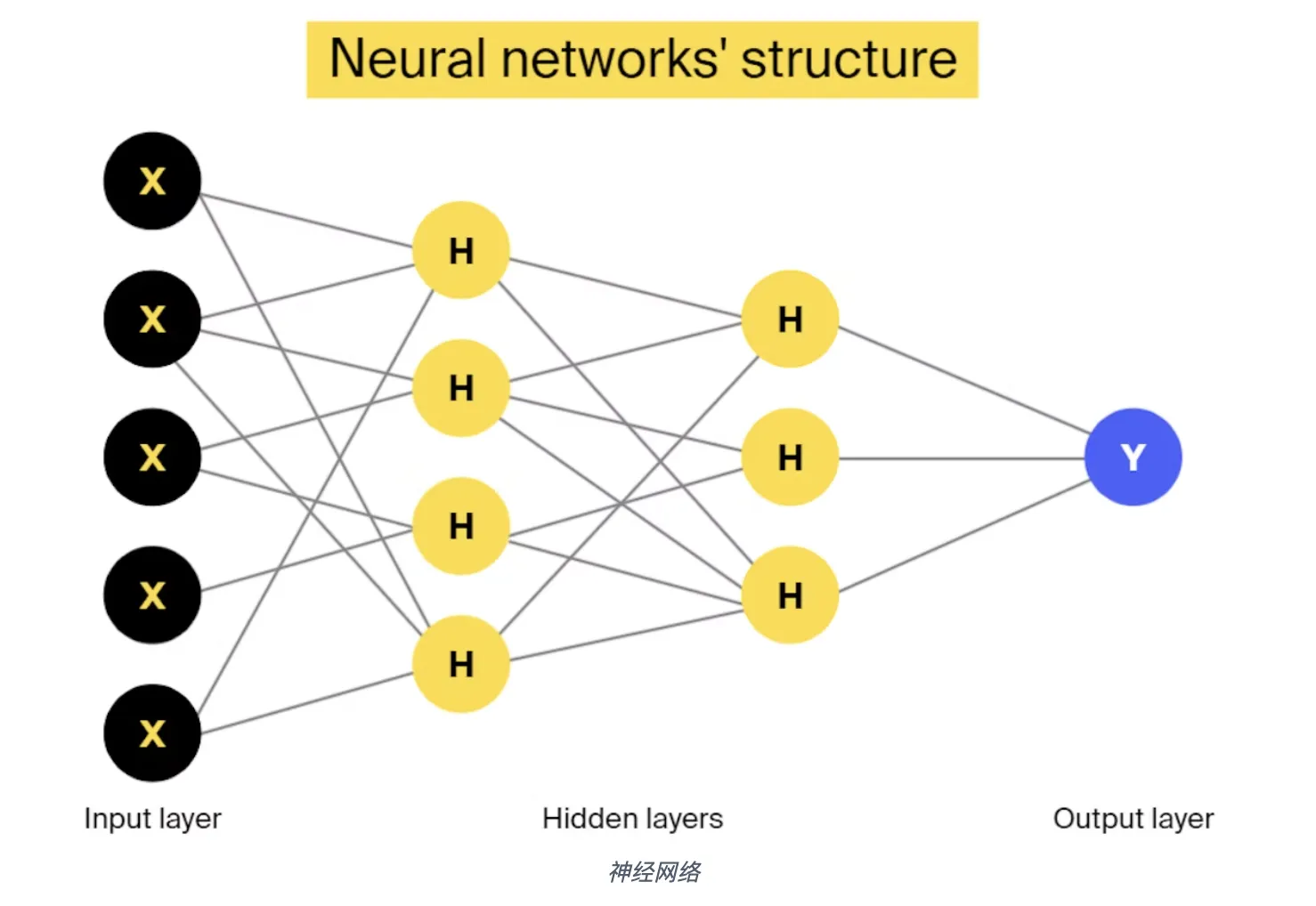
AlphaFold 1展示了神经网络在建模蛋白质折叠机制中的潜力,而AlphaFold 2引入了更具代表性的内部表征,并在模型中嵌入了等变知识。
AlphaFold 3进一步发展,预测蛋白质与其他类型分子的相互作用,从而提供对生命分子相互作用的全面理解。
DeepMind的AlphaProteo在训练时利用大量蛋白质数据以及超过一亿个AlphaFold的结构预测,学习了分子相互作用的复杂性。
通过训练,AlphaProteo学习到了蛋白质分子相互结合的方式。给定目标分子的结构以及优先结合位点,模型就能生成在相应位点结合的候选蛋白质。
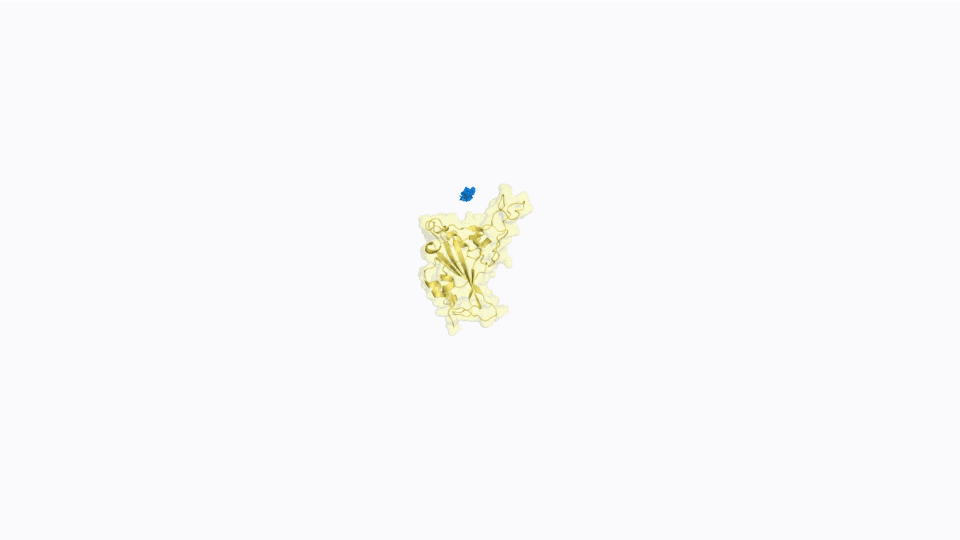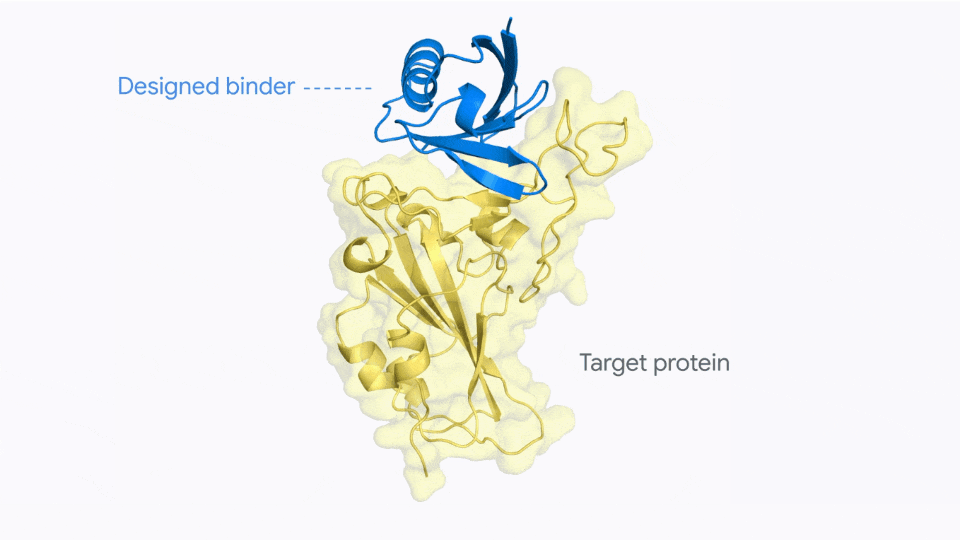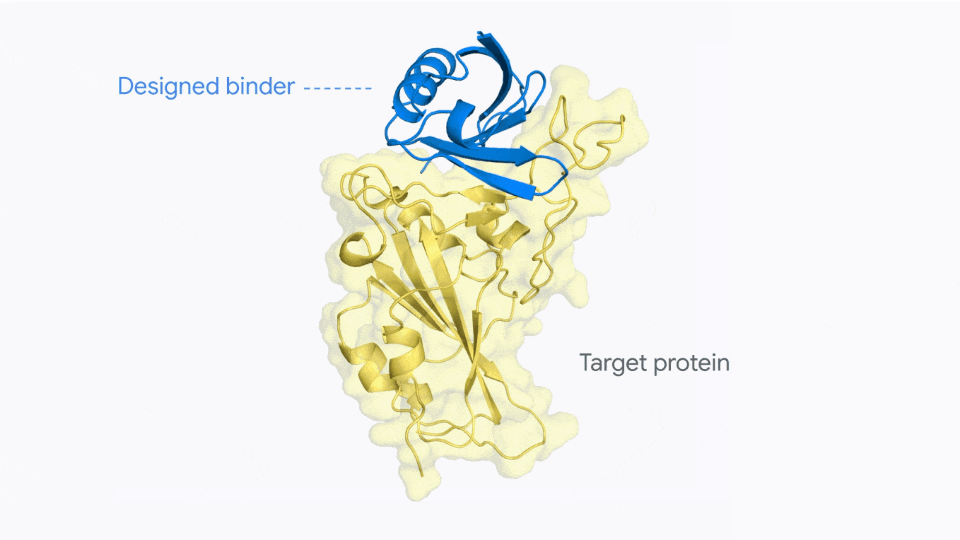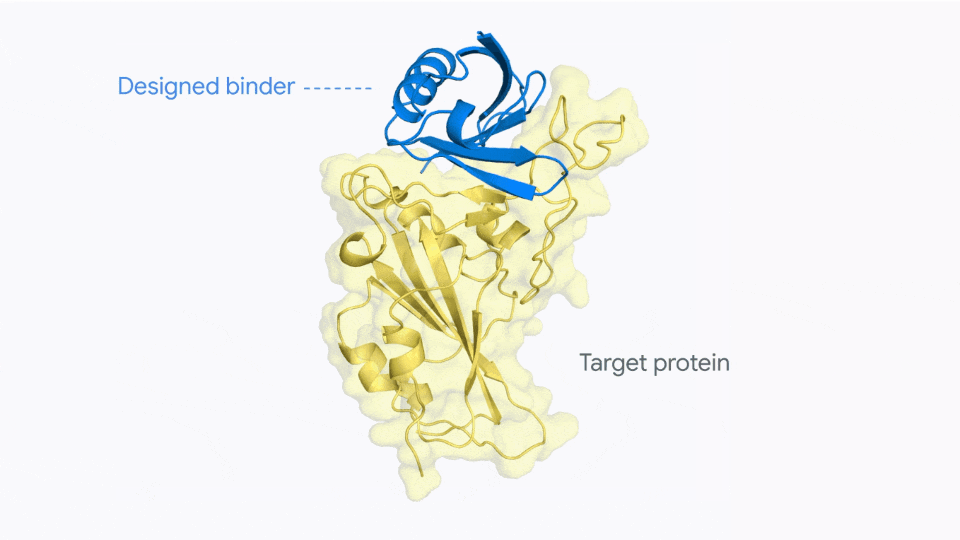
与其前身AlphaFold 主要预测蛋白质结构不同,AlphaProteo能够选择性结合目标(如其他蛋白质)的蛋白质,这对于药物开发、细胞成像和增强作物抗逆性等应用至关重要。
AlphaProteo的功能使其成为生物研究和应用中的变革性方法。

与病毒蛋白质有强亲和力
AlphaProteo生成的蛋白质在与癌症和病毒感染相关的各种目标蛋白中, 展现出了强亲和力 ,这一突破突显了AlphaProteo在实际生物医学挑战中的应用潜力, 使其成为科学和医学领域的变革性工具 。
对制药行业的影响
加速药物发现与开发
制药行业正在经历一场重大的变革,类似DeepMind的AlphaFold这样的人工智能技术,能够预测分子的三维结构,可能导致更多更好设计的临床前资产的产生,从而提高目标验证的效率。
这一技术进步旨在缩短首次人体研究的申请时间。
此外,人工智能工具正在革新药物制造,影响过程设计、规模化、控制及故障检测。
然而,为了充分利用这一更快的药物发现过程,需要临床开发保持同步,以避免延误新治疗方案的交付。

提升药物亲和力与精准医学
谷歌DeepMind的AlphaProteo等人工智能平台在生成新型蛋白质方面显示出显著成果,蛋白质-蛋白质结合亲和力得到了显著提升。
这一突破将显著减少初步实验室实验所需的时间,尤其在创建针对特定靶点的蛋白质结合物时,这对于开发靶向治疗至关重要。
此外,这些人工智能平台的应用可能促成下一代精准医学临床试验设计的出现,尤其是在以患者为中心的策略中,包括N-of-1试验和真实世界数据的使用。
潜在挑战与监管考量
随着这些人工智能驱动的创新在制药行业的普及,它们也带来了独特的挑战,尤其是在监管合规方面。
人工智能方法在药物制造中的实时应用需要强有力的监管框架,FDA和EMA等机构正在制定建议并进行现场检查,以确保合规性。
尽管人工智能在药物发现和生产中可能简化过程, 但它并非万灵药,正如在生成某些蛋白质(如TNFɑ)结合物时的失败所示 。不过,DeepMind仍在不断致力于增强其人工智能工具,以应对未来的复杂目标。
以AlphaProteo为标志的癌症研究
癌症治疗的先进方法
医学界正在见证癌症治疗的革命性转变,靶向疗法通过干扰特定基因和蛋白质来阻止癌症的生长和扩散。
FDA已批准2358种抗癌药物,另有4501种正在研发中。
这些药物分为小分子药物(1016种)和生物技术药物(121种),显示了当前癌症治疗武器库的规模和多样性。
值得注意的是,这些药物中有67种专门针对在癌症通路中至关重要的蛋白质,如EGFR、ERBB2和MTOR。
这种靶向方法符合精准医学的原则,依赖于识别患者肿瘤的独特基因和蛋白质特征,以选择最有效的治疗方案。
AlphaProteo在癌症治疗中的作用
作为一种人工智能设计工具,AlphaProteo展示了创造高结合强度蛋白质结合物的显著能力,其效果超过当前方法3至300倍。
这些结合物对于靶向癌症治疗至关重要,因为它们能以高精度结合与癌症相关的蛋白质。
在测试中,AlphaProteo设计的结合物不仅展现了在癌症治疗中的潜力,还能够抵抗SARS-CoV-2等病毒。
这一突破为更具靶向性的治疗铺平了道路,有望减少副作用,加速药物发现,并可能在研发中节省数十亿成本,同时加快生命拯救治疗的交付。
AlphaProteo等人工智能在药物发现中的应用,可能对癌症患者产生深远影响,尤其是那些罹患侵袭性癌症且治疗选择有限的患者。
生产具有高亲和力的新型蛋白质结合物(例如,针对与糖尿病和癌症相关的VEGF-A的结合物)预示着个性化医学新时代的到来。
这些结合物具有皮摩尔级亲和力并确认了生物功能,标志着蛋白质设计领域的重大进展。
相较于标准治疗,尤其是对经历过多次治疗或剩余选择有限的患者,治疗反应率可能显著提高。
利用AlphaProteo的蛋白质结合物的精确性,临床医生能够借助基因组生物标志物选择有效的免疫疗法或基因导向治疗,从而实现个性化且更有效的治疗方案。
AlphaProteo的训练过程与适应性
训练方法论
DeepMind为AlphaProteo实施了一种复杂的训练方案,利用大量的蛋白质结构和序列作为训练数据。
这种全面的训练使得AI能够识别并做出准确的预测,这在提升系统能力方面发挥了关键作用。
通过吸收海量的信息,AlphaProteo获得了根据不同科学领域特定研究需求量身定制蛋白质的能力,从而促进了从药物发现到农业发展的广泛应用。
为了确保深度学习算法的有效运行,AlphaProteo使用了标准化的蛋白质序列长度。
在实验中,研究人员发现最大长度为500个氨基酸在皮尔逊相关系数(R)和平均绝对误差(MAE)等性能指标之间达到了最佳平衡。
这种标准化使得深度学习系统的输入均匀化,在处理不同数量氨基酸的蛋白质时,通过用零填充较短序列或截断较长序列来实现。
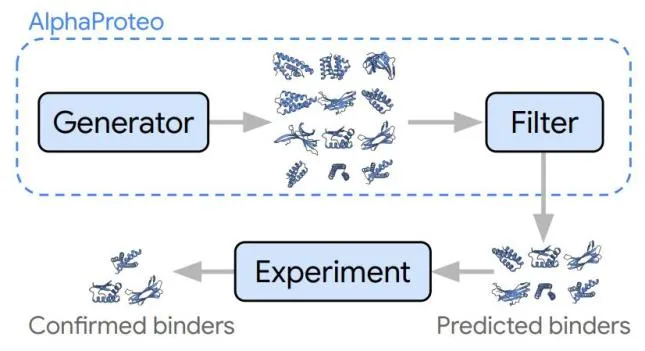
AlphaProteo 工作原理
适应性与潜力
AlphaProteo的适应性突显了其在加快对现有疾病理解和探索大量结构未知的蛋白质的潜力。
尽管在普遍蛋白质数据库(UniProt)中记录了超过1.8亿个蛋白质序列,但在蛋白质数据银行(PDB)中,仅阐明约170,000个蛋白质结构,AlphaProteo就像一台望远镜,使研究人员能够深入未知的生物领域,寻找具有新功能的蛋白质。
此外,AI系统的设计能够适应蛋白质固有的变异性。
例如,在预测蛋白质-配体结合亲和力时,该系统创新性地引入了基于距离的特征,利用独特的分子相互作用和特定残基的蛋白质序列特征,这增强了模型识别复杂结合模式的能力,展现出其在蛋白质设计中应对细微挑战的适应性。
合作努力与改进
尽管面临挑战,例如在创建某些蛋白质(如TNFɑ)结合物方面的困难,AlphaProteo团队依然致力于完善其人工智能。他们努力提高系统的成功率,并扩展其功能范围。
这一目标通过持续的算法改进和与Isomorphic Labs等实体的合作,旨在探索药物设计的新应用。开发者不仅关注技术进步,还关注负责任地传播和使用其人工智能。
他们与外部专家合作,处理与蛋白质设计相关的生物安全问题,并努力确保技术惠及社会,同时降低潜在风险。这体现了他们在快速发展的人工智能驱动的生物技术领域中对负责开发的承诺。
机器学习与计算生物学创新
加速蛋白质设计
机器学习在蛋白质设计领域的应用带来了变革性的变化,使研究人员能够在显著更大的规模上创造新蛋白质和结构。
这不仅加速了这一过程,还通过减少用户输入的需求,使其更加可接近。
约翰霍普金斯大学的教授杰弗里·格雷表示, 这些进展正在革命化生物分子结构预测与设计领域,提升对生物学、健康和疾病的理解 。
DeepMind的AlphaFold正是对预测蛋白质三维结构做出显著贡献的工具,覆盖了DeepMind创始人兼首席执行官德米斯·哈萨比斯所称的“整个蛋白质宇宙”。
这一技术的可接近性,尤其是通过其开源数据库,正在民主化科学研究,促成从药物设计到生物传感器开发的广泛应用。
将机器学习与传统方法结合
像AlphaFold这样的机器学习工具不仅补充了传统的大分子建模方法,甚至在某些方面超越了这些方法。
然而,在兼容性和灵活性方面仍存在挑战,这可能妨碍新技术与现有方法的整合。
通过将机器学习对翻译后修饰(PTMs)的预测融入像Rosetta软件套件这样的工具中,有可能在蛋白质设计中实现广泛的新应用。
这些综合方法最大化了蛋白质的有益特性,例如提高流感血凝素的稳定性和功能,这对于疫苗开发至关重要。
蛋白质-蛋白质结合亲和力预测的未来方向
预测蛋白质-蛋白质结合亲和力对于设计高特异性和高亲和力的目标蛋白质至关重要。
机器学习方法为传统的实验和理论建模方法提供了有前景的替代方案,后者往往耗时并限制了对整个蛋白质空间的探索。
最近在结合亲和力预测方面的机器学习进展显示出可能在如何为各种应用设计蛋白质方面出现范式转变,包括抗体设计和酶工程。
此外,DeepMind的研究引入了利用深度学习与注意机制和集成技术的新方法,以提高对蛋白质-配体结合亲和力的预测准确性,从而增强这些模型在实际应用中的潜力。
随着这些方法的不断发展,它们可能对医学和健康研究的未来产生重大影响,最终可能导致更精确和有效的治疗方案。
未来方向与挑战
个性化癌症治疗
癌症治疗未来的一个重要方向是个性化疗法的发展。
当前,靶向药物常用于传统药物未能产生预期效果的晚期肺癌患者。
由于癌细胞具有独特的基因和蛋白质变化,靶向疗法旨在针对这些特定的基因和蛋白质,以阻止癌症的生长和扩散。
针对非小细胞肺癌(NSCLC)的多个FDA批准的靶向药物,目前选定患者的标准治疗方法涉及通过标准测试识别患者体内的靶向基因和蛋白质。
这种方法旨在限制癌细胞的生长和扩散,同时最小化对健康细胞的损害。
适应性治疗策略
另一个有前景的未来方向是适应性治疗策略。
这些策略旨在根据抗药性癌细胞群体的生长动态调整治疗方案。
传统治疗策略在应对转移性癌症时往往失效,因为会出现药物抗性,而适应性治疗有可能克服这一障碍。然而,适应性治疗的成功受限于目前缺乏考虑患者变异性的个性化方法。
克服药物开发挑战
尽管靶向治疗和适应性治疗策略取得了进展,但药物开发过程仍面临重大挑战。
新药和治疗策略的发现受到成本上升、漫长的开发过程和高失败率的阻碍。
新颖策略,如开放科学伙伴关系,正被考虑以提高这一过程的效率,增强私营部门、学术界与非营利机构之间的合作。
然而,长期维持这些合作关系可能面临挑战。
此外,特别是在这些活动不够协调的国家,亟需强大的学术药物发现网络。
这些网络的发展将促进思想和技术的共享,可能导致更快速、成本效益更高的药物发现过程。