九年级化学下册,影响物质溶解性因素与饱和溶液的相关知识总结
发布时间:2024-09-03
物质的溶解性受多种因素影响,其中最关键的是溶质和溶剂的性质、温度以及压力。这些因素共同决定了物质在给定条件下能够溶解的最大量,即溶解度。
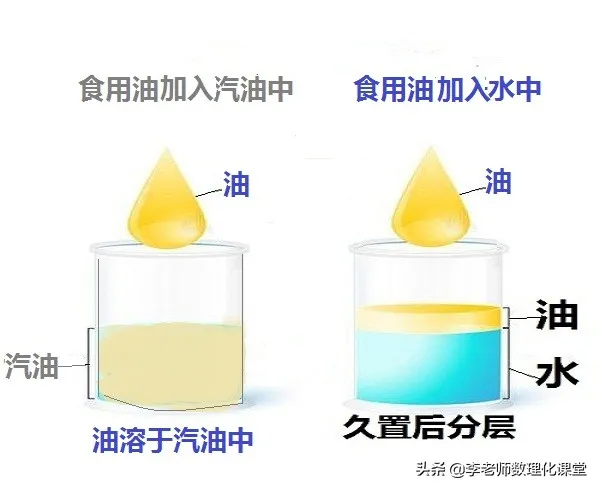
溶质和溶剂的性质是影响溶解性的首要因素。根据“相似相溶”原则,极性相近的物质更容易相互溶解。例如,食盐(一种离子化合物)能在水中溶解,却不能在乙醇中溶解;而油脂(一种非极性共价化合物)则相反,它不能在水中溶解,却能在乙醇中溶解。这一原理可以通过简单的实验验证:将食盐和油脂分别加入水和乙醇中,观察其溶解情况。
温度对溶解度的影响则更为复杂。大多数固体物质的溶解度随温度升高而增加,如硝酸钾。但也有例外,如氢氧化钙的溶解度随温度升高而降低。对于气体而言,其溶解度通常随温度升高而降低。这一规律可以用勒沙特列原理来解释:溶解过程通常是吸热的,因此升高温度有利于溶解;但对于放热的溶解过程,升高温度则会抑制溶解。
压力对固体和液体溶质的影响较小,但在某些情况下仍不可忽视。例如,在矿业中,硫酸钙的溶解度会随压力降低而增加,可能导致油田和油井沉淀结垢。对于气体溶质,压力的影响则更为显著。根据亨利定律,气体的溶解度与其分压成正比。这就是为什么打开汽水瓶时会有气体逸出——瓶盖打开后,压力降低导致二氧化碳溶解度下降。
当物质达到最大溶解量时,溶液就处于饱和状态。饱和溶液是指在一定温度和压力下,溶质不能继续溶解的溶液。例如,在室温下,20mL水中所能溶解的氯化钠的质量有一个最大值,这个最大质量就是形成氯化钠饱和溶液时所能溶解的质量。溶解度通常用“在100g溶剂中所能溶解的溶质质量”来表示,或者用物质的量浓度(mol/L)来表示。
溶解度与温度的关系可以用溶解度曲线来表示。通过观察溶解度曲线,我们可以查出某物质在不同温度时的溶解度,比较不同物质在同一温度时溶解度的大小,以及了解物质的溶解度随温度变化的规律。
了解溶解性和饱和溶液的概念在日常生活中有许多应用。例如,用海水晒盐就是利用了溶解度随温度变化的原理。首先将海水引入蒸发池,通过风吹和日晒使水分部分蒸发;到一定程度后再引入结晶池,继续风吹和日晒,海水就会慢慢成为食盐的饱和溶液;再晒,食盐晶体就会逐渐从海水中析出,得到粗盐。
另一个例子是制作糖浆。通过加热糖水溶液,可以提高糖的溶解度,从而制得浓度更高的糖浆。当溶液冷却后,多余的糖会结晶析出,这就是我们常见的“过饱和”现象。
总之,溶解性是一个复杂的化学现象,受到多种因素的影响。通过理解这些影响因素,以及饱和溶液的概念,我们可以更好地控制和利用溶解过程,在日常生活和工业生产中发挥其重要作用。