为什么学生易混淆“元素和离子”,其原因是没有正确把握这些概念
发布时间:2024-09-16
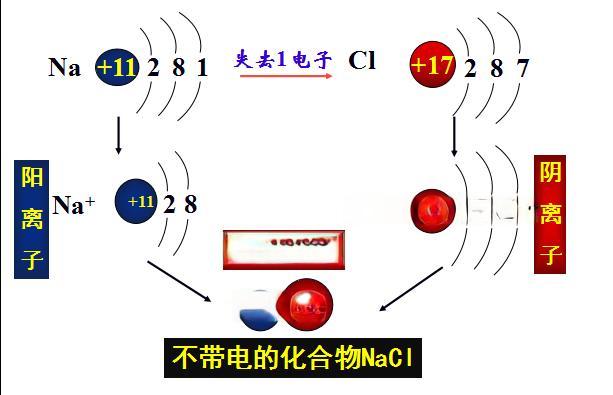
化学元素和离子是化学学习中的两个基本概念,然而许多学生常常将它们混淆。这种混淆不仅影响了对化学知识的理解,还可能导致在解题和实验中出现错误。要正确区分这两个概念,我们需要从它们的历史起源和发展中寻找答案。
元素的概念可以追溯到古希腊时期。公元前450年左右,恩培多克勒提出了著名的四元素说,认为世界由土、气、水、火四种元素组成。这一理论虽然不够精确,但为后世化学家提供了思考物质组成的框架。到了17世纪,英国科学家波义耳在1661年出版的《怀疑派的化学家》中提出了现代化学元素的概念雏形,他质疑了传统的四元素理论,认为物质是由不可再分的基本单元——即后来被称为“元素”的物质组成的。
元素的现代定义是在19世纪确立的。1803年,英国科学家道尔顿提出了原子论,定义了元素是具有相同原子组成的纯净物质。1841年,贝齐里乌斯根据硫、磷等元素能以不同形式存在的事实,创立了同素异形体的概念,进一步明确了元素和单质的区别。19世纪后半叶,门捷列夫建立了化学元素周期系,明确指出元素的基本属性是原子序数。
相比之下,离子的概念是在元素概念的基础上发展起来的。1897年,汤姆逊发现了电子,开启了对原子结构的深入研究。1913年,莫塞莱通过X射线光谱学研究发现了原子序数的概念,并证明原子序数而非相对原子质量决定了元素在周期表中的位置。这一发现极大地推动了周期表的现代化进程,也为理解离子的概念奠定了基础。
元素和离子的本质区别在于电荷。元素是指具有相同核电荷数(即质子数)的一类原子的总称,而离子则是指带有电荷的原子或原子团。当一个原子失去或获得电子时,它就变成了一个带电的粒子,即离子。例如,钠原子(Na)失去一个电子后变成钠离子(Na+),氯原子(Cl)获得一个电子后变成氯离子(Cl-)。
学生容易混淆这两个概念,主要是因为他们没有正确把握它们的本质。元素描述的是原子的种类,而离子描述的是原子或原子团的电荷状态。在化学反应中,元素的种类不会改变,但原子可能会失去或获得电子,从而形成离子。这种变化是化学反应的核心,也是理解化学反应机制的关键。
正确理解元素和离子的概念对学习化学至关重要。它不仅有助于我们理解化学反应的本质,还能帮助我们预测物质的性质和行为。例如,我们知道金属元素倾向于失去电子形成阳离子,而非金属元素倾向于获得电子形成阴离子,这为我们理解离子化合物的形成提供了基础。
总之,元素和离子是化学学习中两个不可或缺的概念。通过了解它们的历史起源和发展,我们能够更好地理解它们的本质区别。记住,元素描述的是原子的种类,而离子描述的是原子或原子团的电荷状态。只有正确把握这两个概念,我们才能在化学学习的道路上越走越远。