氧化还原反应,关键在于掌握“得、低、氧、还;失、高、还、氧”
发布时间:2024-09-18
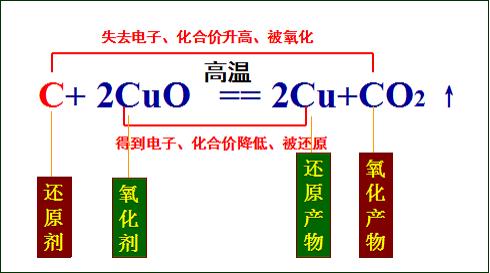
氧化还原反应是化学世界中的一场精彩“电子游戏”。在这场游戏中,原子们通过得失电子来改变自己的“身份”,从而引发各种神奇的化学变化。这种反应不仅存在于实验室的烧杯中,更广泛地影响着我们的日常生活和现代工业。
氧化还原反应的核心在于电子的得失。在反应中,一些原子会失去电子,而另一些则会获得电子。这种电子的转移导致了原子氧化数的变化,从而引发化学反应。例如,当我们看到铁制品生锈时,实际上就是铁原子在空气中与氧气发生氧化还原反应,形成了氧化铁。
要判断一个反应是否属于氧化还原反应,最简单的方法是看元素的氧化数是否发生变化。如果反应前后某些元素的氧化数发生了变化,那么这就是一个氧化还原反应。例如,在反应2H2 + O2 → 2H2O中,氢元素的氧化数从0变为+1,氧元素的氧化数从0变为-2,因此这是一个氧化还原反应。
氧化还原反应在我们的日常生活中扮演着重要角色。当我们呼吸时,身体内的葡萄糖通过氧化还原反应释放能量,维持我们的生命活动。在烹饪过程中,食物的颜色和味道的变化也往往与氧化还原反应有关。例如,切开的苹果变色就是由于其中的酚类物质被氧化。
在工业生产中,氧化还原反应更是不可或缺。金属的冶炼、电池的工作、化肥的生产等都离不开氧化还原反应。例如,在炼铁过程中,氧化铁(Fe2O3)通过与一氧化碳(CO)反应,被还原成金属铁(Fe),同时产生二氧化碳(CO2)。这个反应不仅为我们提供了大量铁材料,还推动了整个工业革命的发展。
氧化还原反应还与环境保护密切相关。在污水处理过程中,通过控制氧化还原反应可以去除水中的有害物质。例如,使用臭氧(O3)氧化有机污染物,或者使用还原剂去除水中的重金属离子。
随着科技的发展,氧化还原反应在新能源领域也发挥着重要作用。例如,在燃料电池中,氢气和氧气通过氧化还原反应产生电能,为电动汽车提供动力。这种反应不仅效率高,而且几乎不产生污染,是未来能源发展的重要方向。
总的来说,氧化还原反应是化学世界中最基本、最重要的反应类型之一。它不仅解释了我们周围世界的许多现象,也为人类社会的进步提供了强大的动力。通过理解和利用氧化还原反应,我们可以更好地改造自然,创造更美好的生活。